近期,遠大醫(yī)藥(0512.HK)創(chuàng)新管線高質量臨床成果不斷。
除創(chuàng)新溫度敏感性栓塞劑GPN00289完成注冊性臨床研究的全部患者入組,為公司核藥抗腫瘤診療板塊再添競爭優(yōu)勢之外,遠大醫(yī)藥心腦血管精準介入診療板塊也迎來了突破性的產(chǎn)品成果——全球創(chuàng)新型人工血管產(chǎn)品aXess取得關鍵性臨床試驗(aXess EU)的成功數(shù)據(jù),產(chǎn)品展現(xiàn)出了安全性和有效性特征,在各方面均優(yōu)于現(xiàn)行標準療法。
這也意味著,作為一款內源性組織修復產(chǎn)品,aXess有望為終末期腎臟病(ESRD)患者的血液透析治療提供更為安全有效的臨床治療方案,或將刷新當前的治療格局。對于遠大醫(yī)藥而言,這一重大進展也將成為遠大醫(yī)藥心腦血管精準介入診療板塊建設的重要里程碑,將為產(chǎn)品未來臨床開發(fā)及注冊等工作的推進提供切實的數(shù)據(jù)支持。
aXess刷新血液透析治療標準,技術創(chuàng)新突破惠及全球患者
慢性腎臟病(CKD)是全球范圍內的重大健康挑戰(zhàn),根據(jù)國際流行病學的數(shù)據(jù)統(tǒng)計,全球有約8.5億的CKD患者。其中終末期腎臟病(ESRD)為CKD的終末階段,弗若斯特沙利文數(shù)據(jù)顯示,2022年全球已有超1000萬患者受其困擾,預計2030年全球病例數(shù)將增長至近1461萬人,年復合增長率約4.5%。中國ESRD患者的數(shù)量約占全球患者數(shù)量的30%以上,預計2030年將超620萬人。
ESRD患者的腎臟已接近衰竭狀態(tài)或已完全衰竭,需長期依賴透析或是腎移植以維持生命。血液透析作為一種風險低且適用范圍廣泛的治療方式,受到了ESRD患者的普遍青睞。全國血液凈化病例信息登記系統(tǒng)新數(shù)據(jù)顯示,截至2024 年底,我國維持性血液透析(MHD)患者已達102.7萬人。
這也直接帶動了血液透析醫(yī)療器械市場規(guī)模的增長,根據(jù)弗若斯特沙利文數(shù)據(jù),2019年至2022年國內的復合年均增長率約為6.5%,預計至2030年將增加至近484億元。其中,血管通路產(chǎn)品市場占據(jù)重要份額,且增速高于整體市場。
盡管市場需求龐大,但目前常用的血液透析通路——自體動靜脈內瘺(AVF)仍然伴隨著血栓、感染和通暢率不理想等問題,這也直接影響了患者的生存質量及預后。
aXess展現(xiàn)出的優(yōu)異性能,有望解決這一臨床痛點,為患者構建起更為安全高效的“生命線”。其在歐洲18個中心開展的前瞻性研究(aXess EU)結果顯示,與其他動靜脈移植物相比,aXess在主要和次要終點均展現(xiàn)出優(yōu)異的通暢率,且干預次數(shù)更少;與AVF相比,aXess的再干預率更低且具有高抗感染性。
其中,研究的安全性數(shù)據(jù)尤為引人注目。在參與試驗的全部120名患者中,僅出現(xiàn)一例因穿刺感染相關的(部分)人工血管取出事件,證明了產(chǎn)品非常高的抗感染性能。aXess可實現(xiàn)近乎即時的穿刺操作,在超過1.5萬次透析治療中,出血并發(fā)癥發(fā)生率低于0.02%。
更為值得一提的是,此次參與試驗的多數(shù)患者曾有動靜脈移植物或透析瘺管失敗史,或曾依賴中心靜脈導管(CVC)。這些患者原本面臨著嚴峻的健康挑戰(zhàn),而試驗結果的顯著成效,則進一步凸顯了aXess在此類病例中的臨床應用價值。
據(jù)悉,aXess的革命性潛力源于其獨特的內源性組織修復(ETR)技術,該技術借助多孔微結構,可以為患者自體組織修復提供基礎結構框架,并通過患者自身組織對多孔微結構的快速填充,使患者最終形成一條和自身血管一模一樣的“活的”血管,加快透析通路的建立,降低血栓以及相關并發(fā)癥的發(fā)生。
此次aXess EU的研究結果也將為其全球研發(fā)提供進一步的數(shù)據(jù)支撐。目前,aXess在美國獲批開展的關鍵性臨床研究已于2024年11月完成了頭例患者入組,在歐洲開展的關鍵性臨床研究于2025年1月完成了全部患者入組,同時,該產(chǎn)品在中國的注冊工作也在積極地推進中。
aXess的全球開發(fā)不僅有助于公司吸收先進技術,也為產(chǎn)品未來在全球市場的順利拓展奠定了基礎。隨著全球臨床研究的穩(wěn)步推進,該產(chǎn)品未來有望在全球范圍內推廣應用,惠及更多飽受血液透析血管通路問題困擾的患者,為全球慢性腎臟病治療領域帶來革命性的突破,遠大醫(yī)藥也或將憑借該產(chǎn)品在高端醫(yī)療器械領域進一步提升國際影響力。
協(xié)同產(chǎn)品拓寬透析通路,精準介入診療板塊兌現(xiàn)創(chuàng)新產(chǎn)品布局預期
aXess的成功進展是遠大醫(yī)藥心腦血管精準介入診療平臺建設的重要成果,該產(chǎn)品還可與公司另一款創(chuàng)新醫(yī)療器械APERTO® OTW在血液透析領域形成協(xié)同,共同為患者構筑起通暢的透析通路。
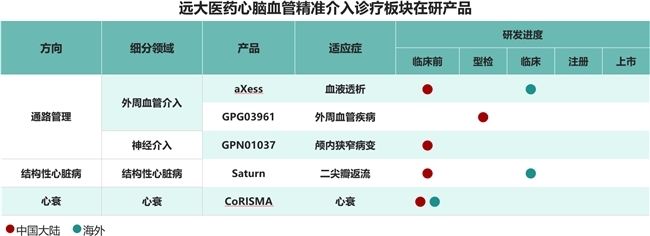
這一產(chǎn)品組合,是遠大醫(yī)藥在心腦血管精準介入領域結構性布局的垂向拓展。實際上,目前公司在該領域秉承“精準治療”理念,圍繞通路管理、結構性心臟病及心衰三個方向進行多方位布局,已搭建起包含超過30款產(chǎn)品的高端醫(yī)療器械產(chǎn)品集群,其中通路管理方向已有22款產(chǎn)品在中國獲批上市,結構性心臟病已有1款產(chǎn)品在中國獲批上市。
尤其在今年,公司心腦血管精準介入診療板塊已進入商業(yè)收獲期,多款產(chǎn)品成功獲批上市。多極腎動脈射頻消融系統(tǒng)鉑睿時Iberis™于2025年2月獲得國家藥監(jiān)局批準在中國上市,并已成功完成上市后臨床應用。該產(chǎn)品是目前獲得歐盟CE認證且具備橈動脈與股動脈雙入路設計的腎動脈去交感神經(jīng)消融術(RDN)產(chǎn)品,相關研究成果已在國際心血管學術期刊Circulation(影響因子:35.5)上全文發(fā)表。
此外,公司經(jīng)導管二尖瓣夾系統(tǒng)NeoNova®和冠脈沖擊波系統(tǒng)DEEPQUAKE-C™分別于2025年2月和2025年6月獲得國家藥監(jiān)局批準在中國上市。其中NeoNova®上市后已迅速在全國多中心開啟頭批商業(yè)化植入,其手術操作的便捷性及術后效果深受臨床專家好評。與此同時,其他產(chǎn)品也在積極推進中國臨床注冊工作,公司力爭在未來年度實現(xiàn)創(chuàng)新產(chǎn)品分階段分梯次上市,帶動心腦血管精準介入診療板塊業(yè)務穩(wěn)定增長。
持續(xù)涌現(xiàn)的產(chǎn)品研發(fā)和商業(yè)化進展的背后,是公司扎實的技術平臺建設。目前,遠大醫(yī)藥在心腦血管精準介入診療板塊已實現(xiàn)“無源+有源”創(chuàng)新器械平臺的全面建設,其中,武漢光谷有源器械研發(fā)生產(chǎn)基地和常州無源器械研發(fā)生產(chǎn)基地,以及聚焦結構性心臟病領域的上海器械研發(fā)中心均已投入使用。同時,遠大醫(yī)藥積極拓展國際合作,與美國、加拿大、德國、意大利、瑞士等多國臨床中心和研發(fā)平臺建立技術合作關系,“Go Global”全球化創(chuàng)新戰(zhàn)略布局穩(wěn)步推進。
產(chǎn)品及技術平臺發(fā)展的豐碩成果,不僅展現(xiàn)了遠大醫(yī)藥在高端醫(yī)療器械領域的全球研發(fā)實力,也體現(xiàn)了公司對于患者臨床需求的深刻理解。隨著aXess等創(chuàng)新產(chǎn)品的順利開發(fā),以及公司“Go Global”戰(zhàn)略的推進,遠大醫(yī)藥在高端醫(yī)療器械領域的發(fā)展前景值得期待,公司有望憑借其創(chuàng)新產(chǎn)品和技術優(yōu)勢,在全球醫(yī)療健康產(chǎn)業(yè)中發(fā)出更強的“中國聲音”,為全球患者帶來更優(yōu)的治療選擇。




評論